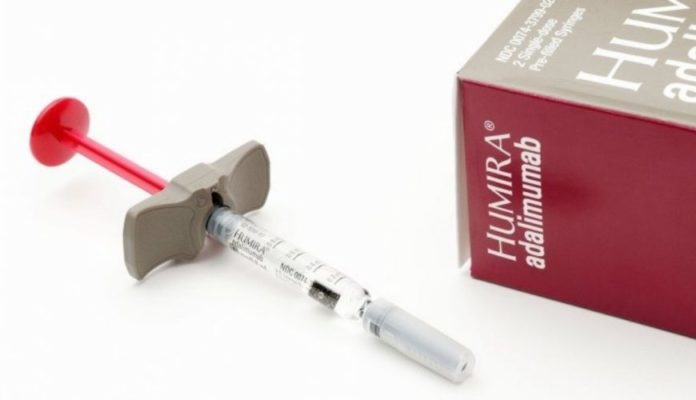

Na semana passada, a Agência Nacional de Vigilância Sanitária (ANVISA) emitiu um comunicado quanto a apreensão de unidades falsificadas comercializadas do medicamento Humira® AC (adalimumabe). O caso está em investigação.
Medicamento falsificado – notificado pela AbbVie
O medicamento Humira® contém o princípio ativo adalimumabe, um anticorpo monoclonal anti-TNFα. Seu uso é bem estabelecido na Reumatologia para o tratamento de doenças como artrite reumatoide, artrite psoriásica, espondilite axial e espondilite anquilosante.
Em 04 de maio (2022), a ANVISA determinou a apreensão de lotes do medicamento Humira® AC 40 mg, na forma de seringas preenchidas (lote 1146607 – data de fabricação 05/2021, validade 01/2023).
A indústria farmacêutica responsável pelo registro do medicamento (Abbvie) comunicou quanto a falsificação do produto. As diferenças observadas em relação ao medicamento original foram: (1) fechamento do blister; (2) cor da marca de segurança; (3) cor e tamanho da fonte do blister; (4) diferentes dimensões de embalagem; e (5) ausência da marcação em braile.
No site na ANVISA é possível obter mais detalhes, incluindo fotos do produto adulterado. Para saber mais, clique aqui, ou acesse os links nas referências.
Quais as recomendações?
A recomendação atual da agência regulamentadora é que os serviços de saúde, ao identificarem as unidades falsidades, não utilizem os produtos e comuniquem via serviço NOTIVISA. Em caso de dúvidas, é possível entrar em contato com o serviço de atendimento ao consumidor da Abbvie Farmacêutica (0800-022-2843).
—–
Referências:
RESOLUÇÃO RE Nº 1.413, DE 02 DE Maio DE 2022. DIÁRIO OFICIAL DA UNIÃO. Publicado em: 04/05/2022 | Edição: 83 | Seção: 1 | Página: 560
Agência Nacional de Vigilância Sanitária (ANVISA). Anvisa determina apreensão e proibição de unidades falsificadas do medicamento Humira AC. Publicado em 04/05/2022. Atualizado em 09/05/2022.
Para saber mais sobre a bula do medicamento, acesse nosso app WeMEDS®